先说说题外话,今天读到一篇很有意思的文章,明白了我们与影像高手的距离在哪里。作为呼吸科大夫,我们最常见的一手资料除了患者的临床表现,那就是影像了。影像可以给我们提供非常多的信息,比如急性肺水肿、肺栓塞、脓毒血症等等,但是平常我们在读片的时候往往会诊断错误或者不知道这是什么病,而你身边的高手则会心一笑,造成这种情况的原因可以用列线图来解释。
什么是列线图
列线图(Nomogram)可以用于多指标联合诊断或预测疾病发病或进展。近些年来在高质量临床论文中用的越来越多。我们看看下面这张列线图怎么解读。
![图片[1]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/列线图.png)
图中最上面是得分,最下面是总得分和预测风险。比如1个患者的肺CT中结节的放射线特征是0.5,对应最上面的得分是50分,结节的最大直径是10,对应的得分是20,如果结节有分叶,对应的得分是12.5,如果有胸膜牵拉,对应的得分是12.5,总得分是50+10+20+12.5+12.5=105,对应总分下面的腺癌风险是95%。该模型曲线下面积 (AUC) 为 0.91(灵敏度,80%;特异性,83%;准确度,82%;NPV,80%;PPV,83%)。
这个模型主要包括了3个方面的内容,临床特征+影像学特征+放射组学特征。这3种特征综合起来要比单一的预测模型要高。这种临床上简单易懂的模型如果成功应用于临床的话,我们可能都变成“影像高手”了。那么对于一张肺CT来说,你获得的细节特征越多,那么我们脑袋里的“总得分”就会越高,诊断成功率也就越高。所以,归根到底需要掌握更多的影像特征。建议加入我们,共同提高(打一波广告)。
在这儿我们先岔开给大家简单讲一下影像组学这一未来非常有潜能的方向。影像组学(Radiomics)是利用数据挖掘等信息技术,从影像、病理、基因等海量数据中挖掘提取并量化肿瘤海量特征,解析影像与基因和临床信息(分型、疗效和预后等)关联的新方法。
![图片[2]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/放射组学.jpg)
当然,目前在临床应用可能还不现实,待这种影像组学技术进一步发展以后,更有利于肺部疾病的诊断。鉴于目前我们还无法成熟的运用这种列线图模型,因此本文还得从影像学特征出发,查找相关隐球菌的影像表现呈现给读者们。
正文正式开始:
肺隐球菌病是较常见的侵袭性肺部真菌感染性疾病。其致病菌主要是新型隐球菌和哥特隐球菌,是一类在无性繁殖期呈无菌丝的单芽胞酵母样真菌,以腐生方式存在于自然界,可引起人类的机会性感染,大多以呼吸道吸入途径进入机体,以侵犯肺和中枢神经系统为多见。免疫健全及免疫抑制者均可发病,免疫健全者比例高于免疫抑制者。不同的免疫状态下,肺隐球菌病的临床及影像学表现有所不同。免疫健全者临床表现多轻微,肺部病灶多较局限。免疫抑制者临床表现多较重,易播散。
导致人类隐球菌病的隐球菌主要为新生隐球菌(Cryptococcus neoformans)和格特隐球菌(Cryptococcus gattii)。新生隐球菌广泛分布于全球各地,分为格鲁比变种(C. neoformans var. grubii,血清A型)、新生变种(C. neoformans var. neoformans,血清D型)及混合变种(AD hybrid,血清AD型)。格特隐球菌的血清型主要为B型和C型。我国隐球菌病患者感染的格特隐球菌主要为VGI型菌株。土壤是隐球菌寄居的重要场所;鸽子是隐球菌的天然宿主,但并不引起发病,仅在其传播中扮演重要角色。近年来,旅游热带来接触广场鸽子的机会增加可导致隐球菌的传播。家庭宠物(如猫、狗等)也可携带隐球菌,通过直接接触传播。
隐球菌引起人类感染的最常见方式是通过吸入。机体吸入空气中无荚膜或仅有小荚膜的隐球菌孢子后(直径约 1–5 μm)可到达下气道和肺泡,并在胸膜下引起炎症。因此肺隐球菌病典型的CT表现为主要位于胸膜下2 cm以内及两下肺病灶。[1][2]
临床表现
肺隐球菌感染的临床表现缺乏特异性,从无症状到严重的急性呼吸窘迫综合征(ARDS)均有发现,其严重程度通常取决于机体的免疫状态。非免疫抑制患者最常见的症状是咳嗽、咳痰、胸闷及发热等非特异性表现。免疫抑制的肺隐球菌病患者症状较多,容易引起全身播散,病死率高。
实验室检查:
隐球菌荚膜多糖抗原检测多是在临床根据影像怀疑肺隐球菌病的时候进行的检查。研究显示,对于免疫低下的艾滋病患者, CD4+ T细胞计数 <100 cells/mm3的患者,建议常规进行抗原检测。与培养、病理学检查相比,隐球菌抗原检测具有快速简便的优势,同时具有较高的敏感性和极高的特异性。但肺部孤立性病灶的隐球菌抗原阳性率低。有关支气管肺泡灌洗液(BALF)LA的研究证据较少,可考虑作为诊断的补充手段。最新的一项包括肺外隐球菌病的研究发现,重度免疫功能不全的患者组血清荚膜多糖抗原检测(CrAg)检测阳性率高于中度或正常免疫组 [2]。
影像学检查:
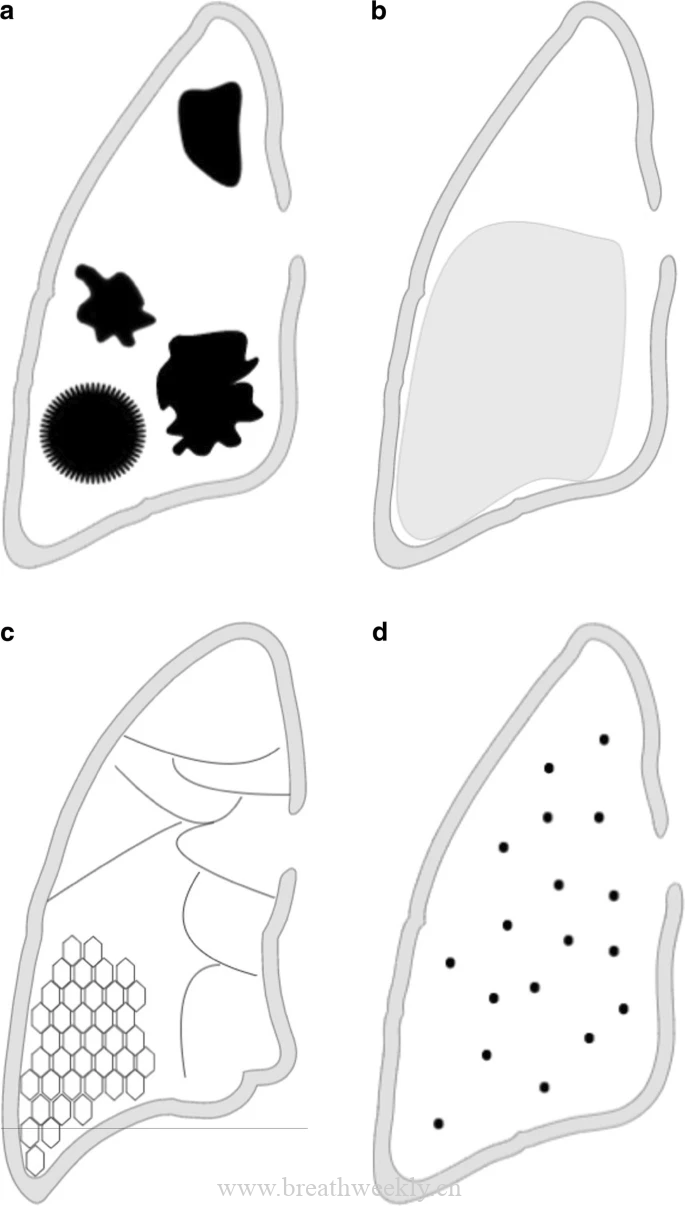
影像学可有多种表现,对于非免疫抑制患者,最常见的发现是胸膜下单个或多个结节,伴或不伴有晕征,较少合并钙化,树芽征,淋巴结肿大或胸腔积液。PET/CT可出现高摄取。对于免疫抑制患者,可有多种CT扫描表现,包括单个或多个结节、节段性实变、空洞、双侧支气管肺炎、肿块样表现、弥漫性粟粒样模式或混合模式。免疫功能低下的患者更常见于近端空气支气管、空洞和晕征的 CT 表现,其胸腔积液更常见。非艾滋病免疫功能低下的患者比免疫功能正常的患者在结节/肿块中出现空洞的频率明显更高[7],磨玻璃影也更常见(p=0.05)[7]。最后我们附上从文献中收集的以结节、实变、空洞、淋巴结肿大、粟粒样表现的影像分类展示。
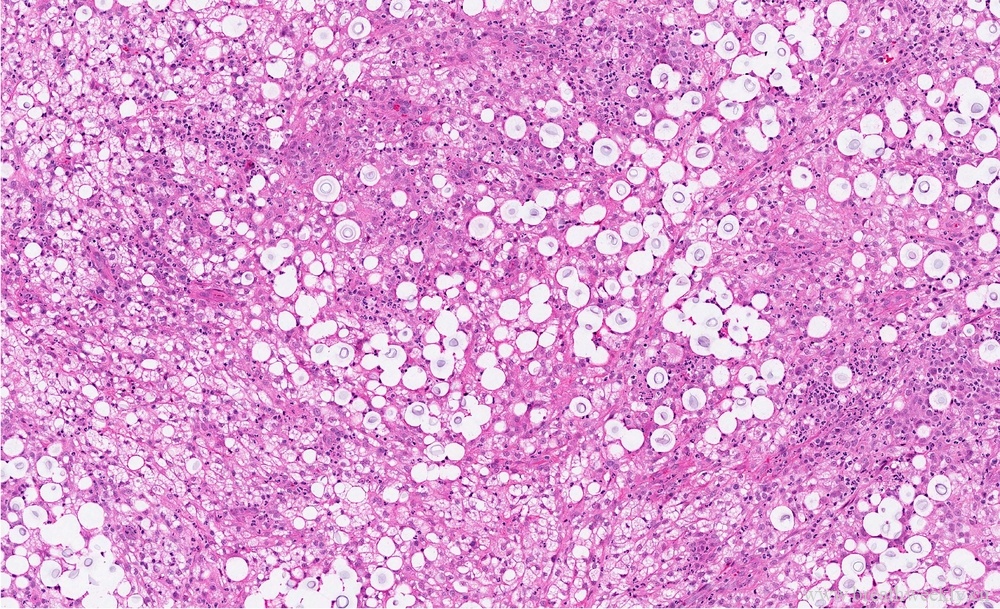
病理检查:
隐球菌所致肉芽肿性炎症,病理一般表现为巨噬细胞、淋巴细胞、浆细胞和多核巨细胞的聚集物。是否形成肉芽肿性病理表现可能与宿主免疫状态以及隐球菌荚膜特征有关。免疫缺陷的隐球菌病理缺乏炎症反应的表现。
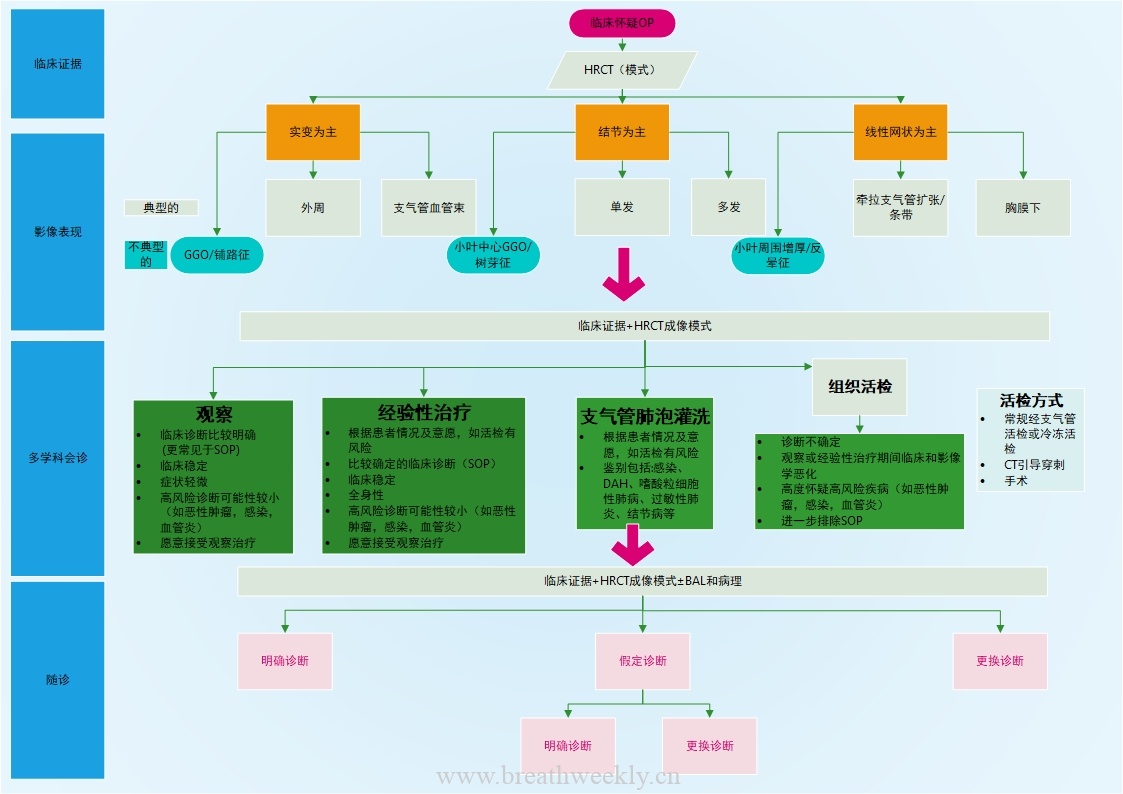
诊断
无菌部位标本病原学涂片及培养阳性、组织病理检查发现隐球菌是确诊的"金标准"。根据修正的EORTC/MSG诊断标准,隐球菌可分为确诊,疑诊或定植[4]。其中查阅相关资料,支气管肺泡灌洗液涂片或培养阳性可作为临床诊断的依据。血清隐球菌荚膜多糖抗原的定性和定量检测在肺隐球菌病的快速诊断中具有较高的价值。近来通过肺泡灌洗液或肺穿刺物进行高通量二代测序等分子生物学技术可应用于临床疑难、危重、特殊病例的病原学检测,对临床常用方法难以确诊或经验性治疗无效的病例具有一定优势。但因真菌破壁技术等客观原因,二代测序用于诊断肺隐球菌病的敏感性有待提高,需进一步探索研究。
![图片[3]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/诊断流程-1024x671.png)
治疗
治疗方案部分选自2017年肺隐球菌病诊治浙江省专家共识(其他相关隐球菌治疗指南或共识已上传至网站,包含相应替代方案,有需要的可以下载)。
| 患者类型 | |
| 无免疫抑制肺隐球菌病患者 | |
| 无症状患者 | 密切观察,氟康唑200~400 mg/d,6个月 |
| 轻至中度症状、无播散患者 | 氟康唑400 mg/d,6~12个月 |
| 重度症状患者 | 诱导治疗为两性霉素B(0.5~1.0 mg/kg/d)联合氟胞嘧啶(100 mg/kg/d),疗程≥4周;巩固治疗为氟康唑400 mg/d,8周;维持治疗为氟康唑200 mg/d,6~12个月 |
| 免疫抑制肺隐球菌病患者 | |
| 无症状、轻至中度症状、无播散患者 | 氟康唑400 mg/d, 6~12个月 |
| 重度症状患者 | |
| HIV患者 | 诱导治疗为两性霉素B(0.5~1.0 mg/kg/d)联合氟胞嘧啶(100 mg/kg/d),疗程≥2周;巩固治疗为氟康唑400 mg/d,疗程≥8周;维持治疗为氟康唑200 mg/d,治疗≥12个月或直至宿主免疫功能的恢复。 |
| 器官移植患者 | 诱导治疗为两性霉素B脂质体复合物(3~4 mg/kg/d)联合氟胞嘧啶(100 mg/kg/d),疗程≥2周;巩固治疗为氟康唑400 mg/d,≥8周;维持治疗为氟康唑200~400 mg/d治疗,6~12个月 |
| 其他患者 | 诱导治疗为两性霉素B(0.5~1.0 mg/kg/d)联合氟胞嘧啶(100 mg/kg/d),疗程≥4周;巩固治疗为氟康唑400 mg/d,8周;维持治疗为氟康唑200 mg/d,6~12个月 |
无论是免疫功能抑制或正常患者,伊曲康唑、伏立康唑和泊沙康唑均可作为不耐受氟康唑或更多常规治疗无效的补救治疗。对于氟康唑治疗后复发患者,氟康唑的敏感性会下降,伊曲康唑、伏立康唑和泊沙康唑等可作为氟康唑治疗失败后的补救措施。对于常规药物治疗症状或体征持续无缓解,影像提示肺部病灶持续存在的患者,可考虑外科手术切除治疗,而不是继续抗真菌治疗或予以观察。术后给予抗真菌治疗至少2个月,以避免造成隐球菌播散。因误诊为肿瘤或其他疾病而行手术切除者,最后确诊为单一的肺隐球菌病的患者,如果这些患者无症状,且血清隐球菌抗原阴性,建议密切观察。在 12 个月的随访中,大多数 (76%) 患有肺隐球菌病的免疫功能正常的患者在治疗后血清 CrAg 滴度从 >1:32 缓慢下降至阴性。CrAg 在成功治疗后可能会持续数月。因此,血清 CrAg 不能用作预后工具或评估对肺隐球菌病治疗的反应。
另外近期pubmed发布了一篇罕见正常免疫功能患者在治疗隐球菌病过程中出现类免疫重建样反应(IRIS)的病例(图15)。其中要学习3点内容包括:1、隐球菌免疫重建炎症综合征 (c-IRIS) 甚至可以在免疫功能正常的宿主中发生,但在 CNS 中比在肺部更常见。2、孤立性肺隐球菌病可发生在免疫功能正常的宿主中,无需特定的抗真菌治疗即可消退。然而,如果肺隐球菌患者接受抗真菌治疗并表现出放射学恶化,则考虑 c-IRIS 的可能性。3、类固醇可用于治疗 c-IRIS,但推荐剂量和持续时间尚不清楚,必须根据临床反应进行调整。对于由 IRIS 引起的主要 CNS 或肺部并发症的患者,这些指南建议考虑使用可接受剂量范围为 0.5-1.0 mg/kg/天的泼尼松等效剂量的皮质类固醇,或者对于更严重的疾病可能使用更高剂量的地塞米松。IDSA 建议继续使用抗真菌药,但没有给出类固醇疗程的明确建议,建议开始使用 2-6 周的类固醇是合理的[3]。
从文献中收集的以结节、实变、空洞、淋巴结肿大、粟粒样表现的影像分类展示。
1、以结节为主要表现
![图片[4]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图1-2.jpg)
![图片[5]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图2-2.jpg)
![图片[6]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图4-2-1024x525.jpg)
![图片[7]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图8-3.jpg)
![图片[8]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图-13-1024x705.jpg)
2、磨玻璃影或实变表现
![图片[9]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图7-3.jpg)
![图片[10]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图6-3.jpg)
![图片[11]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图9-3.jpg)
![图片[12]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图3-4.jpg)
![图片[13]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图10-3.jpg)
3、空洞
![图片[14]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图5-2.jpg)
4、粟粒样表现
![图片[15]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图-11.jpg)
![图片[16]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图-14.gif)
5、淋巴结肿大
![图片[17]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图12-3.jpg)
![图片[18]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图17-2.jpg)
6、其他
![图片[19]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图-15-1024x474.jpg)
![图片[20]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/图-16.jpg)
参考文献:
[1] 谷雷,文文,赖国祥. 肺隐球菌病诊治进展. 中华医学杂志,2020,100(04):317-320. DOI:10.3760/cma.j.issn.0376-2491.2020.04.017
[2] 浙江省医学会呼吸病学分会. 肺隐球菌病诊治浙江省专家共识. 中华临床感染病杂志,2017,10(5):321-326. DOI:10.3760/cma.j.issn.1674-2397.2017.05.001
[3] Perfect JR, Dismukes WE, Dromer F, Goldman DL, Graybill JR, Hamill RJ, Harrison TS, Larsen RA, Lortholary O, Nguyen MH, Pappas PG, Powderly WG, Singh N, Sobel JD, Sorrell TC. Clinical practice guidelines for the management of cryptococcal disease: 2010 update by the infectious diseases society of america. Clin Infect Dis. 2010 Feb 1;50(3):291-322. doi: 10.1086/649858. PMID: 20047480; PMCID: PMC5826644.
[4] Setianingrum F, Rautemaa-Richardson R, Denning DW. Pulmonary cryptococcosis: A review of pathobiology and clinical aspects. Med Mycol. 2019 Feb 1;57(2):133-150. doi: 10.1093/mmy/myy086. PMID: 30329097.
[5] Wu HH, Chen YX, Fang SY. Clinicopathological features of isolated pulmonary cryptococcosis in HIV-negative patients. J Int Med Res. 2020 Jun;48(6):300060520927877. doi: 10.1177/0300060520927877. PMID: 32527202; PMCID: PMC7294504.
[6] Taniwaki M, Yamasaki M, Ishikawa N, Kawamoto K, Hattori N. Pulmonary cryptococcosis mimicking lung cancer. Lancet Infect Dis. 2019 Sep;19(9):1033. doi: 10.1016/S1473-3099(19)30278-6. PMID: 31478508.
[7] Sui X, Huang Y, Song W, Zheng F, Wang X, Xu X, Wang Z, Jiang J, Jin Z. Clinical features of pulmonary cryptococcosis in thin-section CT in immunocompetent and non-AIDS immunocompromised patients. Radiol Med. 2020 Jan;125(1):31-38. doi: 10.1007/s11547-019-01088-8. Epub 2019 Oct 5. PMID: 31587180.
[8] Deng H, Zhang J, Li J, Wang D, Pan L, Xue X. Clinical features and radiological characteristics of pulmonary cryptococcosis. J Int Med Res. 2018 Jul;46(7):2687-2695. doi: 10.1177/0300060518769541. Epub 2018 May 30. PMID: 29848126; PMCID: PMC6124262.
[9] Hu Y, Ren SY, Xiao P, Yu FL, Liu WL. The clinical and radiological characteristics of pulmonary cryptococcosis in immunocompetent and immunocompromised patients. BMC Pulm Med. 2021 Aug 13;21(1):262. doi: 10.1186/s12890-021-01630-3. PMID: 34389002; PMCID: PMC8361630.
[10] Rigby AL, Glanville AR. Miliary pulmonary cryptococcosis in an HIV-positive patient. Am J Respir Crit Care Med. 2012 Jul 15;186(2):200-1. doi: 10.1164/ajrccm.186.2.200. PMID: 22798420.
[11] Fujimoto S, Oda N, Fujioka Y, Mitani R, Takata I. An Elderly Patient with Pulmonary Cryptococcosis with Mediastinal Lymphadenopathy Who Was Successfully Treated with Amphotericin B and Flucytosine. Intern Med. 2020 Oct 15;59(20):2547-2551. doi: 10.2169/internalmedicine.4753-20. Epub 2020 Jun 23. PMID: 32581163; PMCID: PMC7662044.
[12] Wang Y, Gu Y, Shen K, Cui X, Min R, Sun S, Feng C, Chen Y, Wang L, Cao M, Yang J, Yao J, Xu J, Lin D, Tao Y, Ma G, Shi J, Chen B, Ni Y, Zhong H, Shi Y, Su X. Clinical features of cryptococcosis in patients with different immune statuses: a multicenter study in Jiangsu Province-China. BMC Infect Dis. 2021 Oct 8;21(1):1043. doi: 10.1186/s12879-021-06752-x. PMID: 34625036; PMCID: PMC8499499.
(部分图片来源于网络,做学习交流用,无商业目的,如果侵犯到您的权益,请联系删除)
(欢迎关注公众号)
![图片[21]-肺隐球菌病管理 | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/04/扫码_搜索联合传播样式-标准色版-1.png)






暂无评论内容