引言
慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是一种以气流受限为特点的常见呼吸系统疾病。40岁或以上人群的COPD发生率约为10%,但患病率因不同国家而异,且随年龄增长而升高。在美国,COPD一直稳居死亡原因的榜首,每年有超过120,000人死于该病;在COVID-19大流行之前,COPD是全球第三大死亡原因。COPD患病率高且为慢性病程,患者频繁就诊、频繁因急性发作住院,并需要长期治疗(如,辅助供氧、药物),因此使用了大量医疗资源。
定义
COPD及其主要亚型(肺气肿、慢性支气管炎和慢性阻塞性哮喘)的定义,以及导致气流受限的密切相关疾病之间的相互关系,是理解一系列患者临床表现的基础。
COPD — 慢性阻塞性肺疾病全球倡议(Global Initiative for Chronic Obstructive Lung Disease, GOLD)是由美国国家心脏、肺和血液研究所(National Heart, Lung, and Blood Institute, NHLBI)和WHO共同发起的项目,其对COPD的定义如下:
“COPD是一种可预防和治疗的常见疾病,以持续性呼吸系统症状和气流受限为特征,通常由伤害性颗粒或气体显著暴露引起的气道和/或肺泡异常所致,而且受肺发育异常等患者因素影响。严重共存疾病可能会影响并发症发生率和死亡率。”
慢性支气管炎 — 慢性支气管炎定义为连续2年每年慢性咳痰3个月,并排除了慢性咳嗽的其他病因(如,支气管扩张)。慢性支气管炎可能在气流受限之前或之后出现。尽管上述症状持续时间的规定有一定随意性,但该定义已被许多研究所采用。即使没有气流阻塞,吸烟者也可能会在早至36岁时就出现慢性支气管炎症状,并且这些症状与发作发生率更高相关。与从不吸烟者相比,当前吸烟者和既往吸烟者气道黏液的浓度升高(MUC5AC和MUC5B);与GOLD分期(表 1)相似但没有慢性支气管炎症状的患者相比,有症状的患者黏液浓度也升高。
表1
![图片[1]-慢性阻塞性肺疾病COPD | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/09/1663924474-image.png)
![图片[2]-慢性阻塞性肺疾病COPD | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/09/1663919508-image.png)
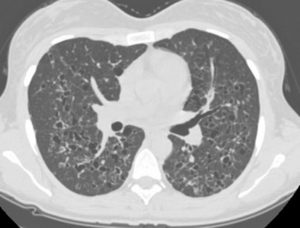
肺气肿 — 肺气肿是病理学术语,用于描述有时与COPD有关的某些结构改变。这些改变包括:终末细支气管远端的气腔永久性异常扩张,伴气腔壁破坏,无明显纤维化(即,无肉眼可见的纤维化)。排除明显纤维化是为了区分肺气肿所致的肺泡破坏与间质肺炎所致的肺泡破坏。然而,许多研究发现,轻度COPD患者的肺组织中胶原增加,这提示纤维化可能是肺气肿的一种表现。虽然肺气肿可出现于无气流阻塞的个体,但它在中度或重度气流阻塞的患者中更为常见。
肺气肿的各种亚型见下文,如近端腺泡型、全小叶型与远端腺泡型。
肺气肿可累及终末细支气管远端结构,包括呼吸性细支气管、肺泡管、肺泡囊及肺泡,统称为腺泡。这些结构与相关的毛细血管和间质一起组成肺实质。永久性扩张或破坏的腺泡部位决定了肺气肿亚型。
•近端腺泡型(即,小叶中央型)肺气肿是指位于腺泡中央的呼吸性细支气管异常扩张或破坏,常与吸烟有关,也可见于煤工尘肺。
•全小叶型肺气肿是指腺泡所有部分的扩大或破坏。弥漫性全小叶型肺气肿最常与AAT缺乏有关,但在吸烟者中它也可与近端肺气肿同时出现。(参见 “α-1抗胰蛋白酶缺乏症的临床表现、诊断和自然病程”)
•远端腺泡型(即,间隔旁型)肺气肿主要累及肺泡管。远端腺泡型肺气肿可单独发生,也可以与近端腺泡型和全小叶型肺气肿同时出现。在年轻成人中,孤立的远端腺泡型肺气肿通常与自发性气胸相关。
哮喘 — 全球哮喘防治创议(Global Initiative for Asthma, GINA)对哮喘的定义为:“哮喘是多种细胞和细胞组分参与的气道慢性炎症性疾病。慢性炎症与气道反应性相关,后者会引起反复发作的哮鸣、呼吸急促、胸闷和咳嗽(特别是在夜间或清晨出现)。这些发作常与肺内广泛但不一的气流阻塞相关,这种气流阻塞常自行缓解或经治疗缓解。”
哮喘、慢性支气管炎和肺气肿之间的相互关系 —COPD不同亚型相互关系的要点包括:
●气流阻塞完全可逆的哮喘患者不属于COPD。
●气流阻塞不能完全缓解的哮喘患者有COPD。这类COPD患者的病因和发病机制可能与慢性支气管炎或肺气肿患者不同。
●有气流阻塞的慢性支气管炎和肺气肿常同时发生。其中部分患者也可能有哮喘。
●哮喘患者的慢性咳嗽可自发出现,也可能因有害物质暴露引起(如,香烟烟雾、变应原)。这类患者常称为喘息性支气管肺炎患者,但该术语尚未得到临床实践指南正式认可。
●除非有气流阻塞,否则不认为慢性支气管炎和/或肺气肿患者有COPD。
●如果气流阻塞的病因已知或具有特定的病理学(如,囊性纤维化、支气管扩张症、闭塞性细支气管炎),则不属于COPD。但是,这些排除诊断的界定较宽松。
哮喘-COPD重叠 — 许多患者同时具有哮喘和慢性支气管炎/肺气肿的炎症特点,这与不同类型COPD之间存在显著重叠的观念一致。同样地,即使是同一类型的COPD患者,其支气管炎症的特点也有很大差别。虽然有人提出用“哮喘-COPD重叠(asthma and COPD overlap, ACO)”描述同时存在哮喘和COPD特征的气道疾病患者,但该术语仍有争议,目前缺乏普遍认可的单一ACO定义。大多数提出的定义要点包括年龄>40岁、持续气流阻塞,以及哮喘病史或支气管扩张剂逆转试验显示部分可逆。
临床表现
COPD的3个主要症状是呼吸困难、慢性咳嗽和咳痰,最常见的早期症状是劳力性呼吸困难。较少见的症状包括哮鸣和胸闷。不过,所有这些症状都可能单独出现,且程度不一。
COPD患者有3种典型的表现形式:
●对于有极端久坐生活方式但几乎没有主诉的患者,需要仔细询问以发现提示COPD的病史。一些患者会不自觉地通过改变自己的期望和限制活动来避免劳力性呼吸困难。虽然这些患者可能诉乏力,但他们可能不清楚自己活动受限的程度,或者并不知道其活动受限是呼吸系统症状所致。
●有呼吸系统症状的患者通常诉有呼吸困难和慢性咳嗽。最初可能只是在劳力时感到呼吸困难。但呼吸困难最终将变得明显,诱发呼吸困难的劳力强度越来越低,甚至休息时也有呼吸困难。慢性咳嗽的特点是咳痰隐匿地出现,最初在清晨出现,但可能发展到整日咳痰。每日痰量偶尔>60mL。痰液通常为黏液,但在发作时可变为脓痰。
●患者间歇性地出现加重的咳嗽、咯脓痰、哮鸣、乏力和呼吸困难,伴或不伴发热。这类患者的诊断可能难以确定。哮鸣和呼吸困难同时出现可能会被误诊为哮喘。而有类似表现的其他疾病,例如心力衰竭(heart failure, HF)、支气管扩张症或毛细支气管炎,则被常误诊为COPD发作。随着COPD的病情日趋严重,发作的间隔时间将缩短。
COPD患者可能出现体重增加(活动受限所致)、体重减轻(可能是进食时呼吸困难所致)、活动(包括性生活)受限、咳嗽性晕厥或感到抑郁或焦虑。体重减轻通常反映了更晚期疾病,与预后较差相关;但大多数COPD患者有超重或肥胖。
体格检查 — 胸部体格检查结果因COPD的严重程度而异。
●在疾病早期,体格检查可能正常,或仅显示呼气相延长或用力呼气时有哮鸣音。
●随着气道阻塞程度的恶化,体格检查可发现肺过度充气(如,叩诊呈过清音)、呼吸音减弱、哮鸣音、肺底湿啰音和/或心音遥远。重症的特征包括胸廓前后径增大(“桶状”胸),胸部叩诊发现横膈下降且活动受限。
●终末期COPD患者可能会采取一些体位来缓解呼吸困难,如伸出双臂以两手掌或两肘部支撑体重的前倾位。这种姿势可能在检查过程中发现,或可由前臂伸侧表面的老茧或肿胀的滑囊提示。其他体格检查结果包括:颈部和肩胛带的辅助呼吸肌参与呼吸、缩唇呼气、吸气时下几个肋间反常回缩(即,Hoover征)、发绀、重度高碳酸血症所致扑翼样震颤,以及右心衰竭所致肝脏增大和触痛。由于胸内压增高,还可能观察到颈静脉怒张,尤其是呼气时。
●患者可能存在由燃烧烟草中尼古丁和焦油引起的手指黄渍,这可提示持续大量吸烟。
杵状指不是COPD(即使伴低氧血症)的特征,杵状指可提示共存疾病,例如肺癌、间质性肺疾病或支气管扩张症。
诊断
当存在与COPD相符的症状时,如静息时或劳力性呼吸困难、伴或不伴咳痰的咳嗽、进展性活动受限,则可提示诊断为COPD,尤其是有COPD触发因素暴露史(如,烟草烟雾、职业粉尘、室内生物质燃料烟雾)、慢性肺疾病家族史或存在相关共存疾病时。
COPD的诊断由以下表现证实:
●肺量计检查证实气流受限,即FEV1/FVC比值<0.7或<LLN,且吸入支气管扩张剂后不能完全使其逆转。
●无法用其他原因解释患者的症状和气流受限。
●GOLD指南建议,初始FEV1/FVC为0.6-0.8的患者,应重复1次肺量计检查,以证实持续气流受限(FEV1/FVC<0.7或<LLN)
确诊COPD后,下一步要考虑病因。大多数患者的病因是长期吸烟。然而,由于减轻持续暴露可能减缓疾病进展,所以医生须与患者一起回顾潜在哮喘、工作场所暴露、室内生物质燃料使用、肺结核既往史或家族易感性是否是促进因素。
稳定期慢性阻塞性肺疾病的初始药物治疗
对于稳定期COPD患者,主要治疗药物是吸入性支气管扩张剂(β受体激动剂和毒蕈碱拮抗剂),单用、联用或添加吸入性糖皮质激素[即吸入性皮质类固醇(ICS)]均可。应在药物治疗的同时开展非药物治疗,如戒烟、肺康复、疫苗接种和营养支持。
●对于所有COPD患者,我们都推荐按需使用短效支气管扩张剂(如,β受体激动剂和/或毒蕈碱拮抗剂),以缓解呼吸困难间歇性加重。对于正使用长效毒蕈碱拮抗剂(LAMA)的患者,通常使用短效β受体激动剂(SABA)以快速缓解COPD症状。对于未使用LAMA的患者,急救时可给予SABA或SABA+短效毒蕈碱拮抗剂(SAMA)。
●对于症状轻微(即mMRC分级<2级)且急性加重风险低(即每年急性加重0-1次)的A类患者,可使用SABA或SABA-SAMA以缓解症状。
●对于症状更严重(即mMRC分级≥2级或CAT评分≥10分)但急性加重既往史提示急性加重风险低(即每年急性加重0-1次)的B类患者,我们推荐规律使用长效吸入性支气管扩张剂。我们在临床上倾向于使用LAMA而非长效β受体激动剂(LABA)。但根据患者症状和潜在药物不良反应,也可改用一日1次的LABA。
●对于日常生活中症状轻微(即mMRC分级为0-1级或CAT评分<10分)但过去1年急性加重史提示急性加重风险高(即每年急性加重≥2次且有至少1次急性加重导致住院)的C类患者,由于LAMA治疗可降低急性加重率,我们建议初始治疗使用LAMA,而不是LABA。
●对于症状负担较重(即mMRC分级≥2级或CAT评分≥10分)且急性加重风险高(即每年急性加重≥2次且有至少1次急性加重导致住院)的D类患者,我们建议初始治疗使用LAMA,但重度呼吸急促患者(如CAT评分≥20分)可能首选LAMA-LABA联合治疗。可能的例外情况为临床表现或检查结果提示哮喘-COPD重叠的患者;对于这些患者,可能更优选LABA-ICS联用。
若患者有COPD频繁急性加重(如每年≥2次)和/或血嗜酸性粒细胞计数≥300/μL,GOLD策略建议将LABA-ICS规律治疗用作替代方案。宜加入ICS试用一段时间(如1-3个月),若症状、急性加重率和/或肺功能未改善则停用ICS
●随访时应根据治疗反应来调整药物治疗方案。
![图片[3]-慢性阻塞性肺疾病COPD | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/09/1663924370-image.png)
慢性阻塞性肺疾病急性发作的处理
慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)急性发作定义为“一次急性事件,特征为患者的呼吸系统症状恶化,这种恶化超出正常每日变化且引起用药改变。这通常包括以下一种或多种主要症状的急性改变:
●咳嗽频率及严重程度增加
●痰量增加和/或痰液性状改变
●呼吸困难加重
治疗总结
逐步调整辅助供氧量–COPD急性发作导致低氧血症的患者应接受辅助供氧。我们建议逐步调整辅助供氧量至脉搏血氧饱和度达到88%-92%的目标值,而不是采用不调整的高流量氧疗。
●通气支持–无创通气(NIV)可改善大量临床结局,是许多COPD急性发作患者的首选通气支持方式。如果呼吸衰竭患者进行NIV失败、不能耐受NIV或有NIV禁忌证,则需要有创机械通气。用于COPD急性发作患者的NIV和有创机械通气见上文和其他专题。
●短效支气管扩张剂–我们推荐所有COPD急性发作患者接受吸入性短效支气管扩张剂治疗。短效β肾上腺素能受体激动剂(SABA;如沙丁胺醇和左沙丁胺醇)比短效毒蕈碱拮抗剂(SAMA)异丙托溴铵起效更快,因此,SAMA-SABA联合治疗(我们的选择)或单用SABA优于异丙托溴铵单药治疗。
•缓解急性症状的常用剂量为一次2揿、每小时1次、共2-3次,然后根据疗效改为每2-4小时1次。
•在这种急诊科或住院治疗中,沙丁胺醇的常用剂量为通过带有储雾器的MDI给予一次1-2揿(多为2揿,偶尔4揿;90μg/揿)或通过雾化器给予2.5mg(用无菌生理盐水稀释到总量为3mL),每小时1次,给予2-3次,然后按需每2-4小时1次。
•雾化给药时,将异丙托溴铵0.5mg(500μg)与沙丁胺醇2.5mg混合制成3mL溶液,每小时给药1次,连用2-3次,然后按需每2-4小时给药1次。也可使用异丙托溴铵-沙丁胺醇联合软雾吸入器(SMI),一次1揿,约1小时1次,连用2-3次,然后按需每2-4小时1次。
•对于使用短效吸入性支气管扩张剂效果不佳的患者,我们建议静脉给予镁剂。
●全身性糖皮质激素–对于因COPD急性发作而住院的患者,我们推荐使用全身性糖皮质激素治疗(Grade 1B);对于不需要住院的患者,我们也建议使用糖皮质激素(Grade 2B)。对于大多数患者,合理的剂量为泼尼松40-60mg、一日1次或其他等效药物,治疗5-14日。对于即将出现或已出现呼吸衰竭的患者,偶尔会使用更大剂量的糖皮质激素。口服给药的结果与静脉给药总体相近。
●抗生素和抗病毒药物–许多COPD急性发作患者需要抗生素治疗,尤其是因急性发作而需要住院的患者。(流程图 2和流程图 3)流感病毒诱发的急性发作或可给予抗病毒治疗(例如口服奥司他韦或静脉制剂),具体取决于流感发病时间和药敏特征。对COVID-19患者使用COVID-19特异性治疗[例如单克隆抗体、JAK抑制剂、抗IL-6药物和瑞德西韦(remdesivir)]的相关内容见其他专题。
●无明确益处的治疗–尚未证实促黏液活性药物、甲基黄嘌呤类药物和增强痰液清除的机械性方法对COPD急性发作患者有益。
![图片[4]-慢性阻塞性肺疾病COPD | 每周呼吸-每周呼吸](https://www.breathweekly.cn/wp-content/uploads/2022/09/1663926230-image.png)
以上内容,参考uptodate,完整版请到uptodate网站访问,仅为学习交流用,如果侵犯到您的权益,请联系删除!
更详细的治疗可参见我国慢性阻塞性肺疾病诊治指南修订版









暂无评论内容