局部射频消融术作为一种微创技术,其临床应用及技术水平近年来得到了显着改善。在消融方式、手术性能、患者选择等方面取得了一些进展。随着近年来高分辨率CT的使用明显增加了对早期肺癌的诊断。对于那些无法手术的早期非小细胞肺癌(NSCLC)患者,影像引导下的经皮肺肿瘤消融技术可能是一种治疗手段。

近期一项Meta分析表明,手术与消融的1至5年总生存期或癌症特异性生存期没有显着差异。手术与消融相比,1年和2年无病生存期明显更好,但3至5年无病生存期不明显。汇总结果表明,手术切除1期非小细胞仍然是最佳选择。对于不适合手术的 1A 期非小细胞肺癌患者,CT引导的微波或射频消融可能是一种替代方案,可提供有前景的无病生存期和总生存期[1]。另一项对立体定向放射治疗 (SBRT) 和射频消融 (RFA) Meta分析表明[2],射频消融与 SBRT 对总生存期的影响无差异(P>.05)。但是对肿瘤的局部控制率。射频消融在 1、2、3 和 5 年的局部控制率(LCR)(95% 置信区间)为 77% (70 – 85%)、48% (37 – 58%)、55% (47 – 62%) 和 42% ( 30 – 54%),显着低于立体定位放射治疗(SBRT) 97% (96 – 98%)、92% (91 – 94%)、88% (86 – 90%) 和 86% (85 – 88%) ) (P<.001)。根据2021年肺癌诊疗指南来说,IA期非小细胞肺癌首选手术治疗,如果不适合手术可以选择根治性放疗。影像引导的热消融是一种安全有效的治疗方法,长期肿瘤学和生存结果可接受,与 SBRT 和亚肺叶切除术相当。
以下介绍的是射频消融的基本知识和原理,以及相应的适应症,禁忌症和并发症。希望通过这些内容可以对射频消融有初步的了解。
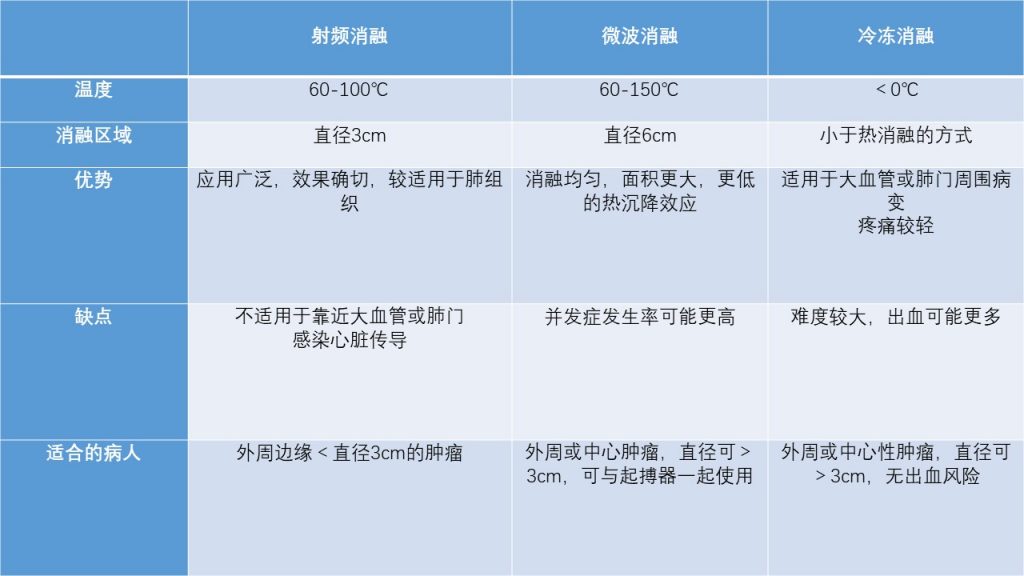
影像引导的经皮肺消融是一种相当于手术和立体定向放射治疗的技术,用于治疗早期非小细胞肺癌或寡转移性肺病患者。可用的方式包括射频消融、微波消融和冷冻消融。
射频消融(RFA) 是一种基于电流的技术,它通过以大约 400 kHz 的频率使肿瘤组织内的离子相互磨擦、碰撞而产生热生物学效应。消融效果是通过主动加热消融设备,将温度逐渐被动地扩散到目标病变中,从而将组织温度升高到 60-100°C。
微波消融(MWA)在消融设备周围产生一个在 915 到 2450 MHz 之间变化的电磁场,导致水分子旋转,最终通过目标病变上的摩擦产生热量,肿瘤组织内的水分子、蛋白质分子等极性分子产生极高速振动,造成分子之间的相互碰撞、相互摩擦,从而导致细胞凝固性坏死。MWA 产生更均匀的消融区,并且温度峰值出现的速度比 RFA 快得多。
冷冻消融(CA)技术包括氩-氦冷冻消融和液氮冷冻系统。氩-氦冷冻消是通过焦耳-汤姆逊(Joule-Thomson)效应,高压氩气可以使靶组织冷却至-140 ℃,氦气可使靶组织从-140 ℃迅速上升至20 ℃-40℃。液氮冷冻消融可以使靶组织冷却至-196 ℃,用无水乙醇升温至80 ℃。整个冻融过程不断重复,直到获得有效消融。CA 的一个限制是,可用的协议描述了需要多达三个冻融循环才能实现正确的消融治疗,这使得该过程比 RFA 和 MWA 更长。
目前的科学证据表明,所有三种消融方式都有相似的治疗效果。因此,在选择消融技术时,需要仔细考虑肿瘤的特点和患者的特点[3]。
目前热消融技术的主要适应症为,1.不能手术的 IA 期NSCLC。具体可分为[5] ①因心肺功能差或高龄不能耐受手术切除;②拒绝行手术切除;③外科切除后又新出现的病灶或遗留病灶,患者无法耐受再次手术或拒绝再次手术;④多发GGN(先消融主病灶,其他病灶根据发展情况考虑再次消融);⑤各种原因导致的重度胸膜黏连或胸膜腔闭锁;⑥单肺(各种原因导致一侧肺缺如);⑦重度焦虑,经心理或药物治疗无法缓解。上述患者需经活检病理证实为AAH、AIS和MIA,对于周围型GGN样IAC患者需排除远处转移。2.某些生物学特征显示预后较好的肺内转移瘤(如肉瘤、肾癌、结直肠癌、乳腺癌、黑色素瘤和肝细胞癌)[4]。如果原发病能够得到有效治疗,可进行肺转移瘤的消融治疗。单侧肺病灶数目≤3个(双侧肺≤5个),多发转移瘤的最大直径≤3 cm,单侧单发转移瘤的最大直径≤5 cm,且无其他部位的转移。对于双侧肺肿瘤,不建议双侧同时进行消融治疗。
绝对禁忌症包括 [5] :①血小板<50×10 9 /L;②有严重出血倾向、短期内不能纠正的凝血功能障碍(凝血酶原时间>18 s,凝血酶原活动度<40%);③严重的肺纤维化和肺动脉高压;④抗凝治疗和(或)抗血小板药物在消融前停用未超过5 d-7 d,贝伐珠单抗末次使用间隔未超过1个月。
相对禁忌症包括[5]①胸腔积液控制不佳者;②肝、肾、心、肺、脑功能严重不全者;③严重贫血、脱水及营养代谢严重紊乱,无法在短期内纠正或改善者;④严重全身感染、高热(>38.5 o C)者;⑤美国东部肿瘤协作组(EasternCooperative Oncology Group, ECOG)评分>3分者;⑥发作期精神病患者;⑦合并其他肿瘤并有广泛转移者,预期生存期<6个月;⑧植入心脏起搏器的患者使用RFA时要在充分评估患者心功能的情况下,可考虑RFA手术期间停止起搏器,手术后恢复起搏器。
并发症,气胸是最常见的并发症,发生率约为30-60%。胸腔积液,消融后可以见到少量胸腔积液,很可能是一种反应性现象。绝大多数无症状,可自行消退。出血,发生率约为3-8%。主要表现为咯血和血胸。感染及空洞形成等其他并发症。空洞大多术后15天-1个月出现,2-4个月后吸收。
总之这种技术是早期无法手术患者及寡转移肺癌患者的一种良好的治疗选择,需要更多的前瞻性的随机对照研究明确消融治疗相对于传统手术,立体定位放射治疗的疗效。
参考文献:[1].Chan MV, Huo YR, Cao C, Ridley L. Survival outcomes for surgical resection versus CT-guided percutaneous ablation for stage I non-small cell lung cancer (NSCLC): a systematic review and meta-analysis. Eur Radiol. 2021 Jul;31(7):5421-5433.
[2].Bi N, Shedden K, Zheng X, Kong FS. Comparison of the Effectiveness of Radiofrequency Ablation With Stereotactic Body Radiation Therapy in Inoperable Stage I Non-Small Cell Lung Cancer: A Systemic Review and Pooled Analysis. Int J Radiat Oncol Biol Phys. 2016 Aug 1;95(5):1378-1390
[3].Páez-Carpio A, et al. Image-guided percutaneous ablation for the treatment of lung malignancies: current state of the art. Insights Imaging. 2021 Apr 29;12(1):57.
[4].叶欣,范卫君,王徽,等. 热消融治疗原发性和转移性肺部肿瘤专家共识(2017年版)[J]. 中国肺癌杂志,2017,20(7):433-445.
[5].叶欣,范卫君,王忠敏,王俊杰,王徽,王俊… & 潘杰.(2021).热消融治疗肺部亚实性结节专家共识(2021年版). 中国肺癌杂志(05),305-322. DOI: 10.3779/j.issn.1009-3419.2021.101.14.





暂无评论内容